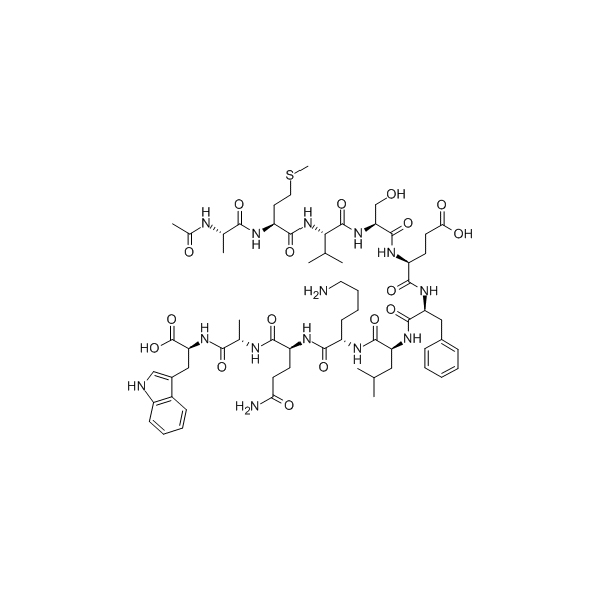
Polybia-MP1/872043-01-1/GT пептид/пептид доставчик
Описание
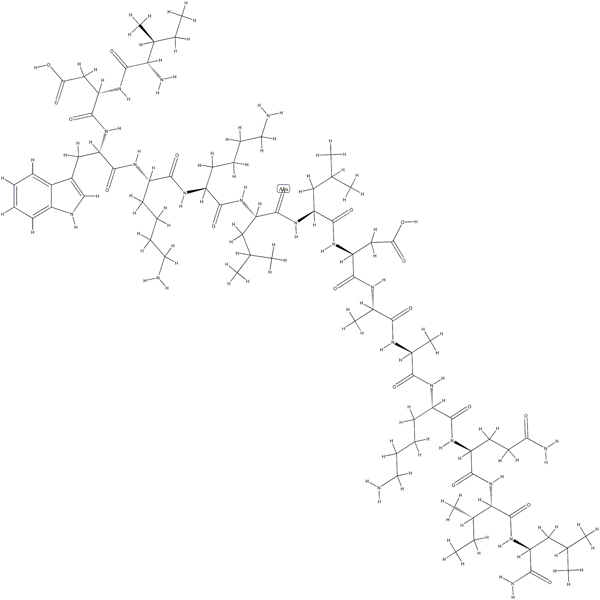
Polybia-MP1 е широкоспектърен бактерициден пептид, екстрахиран от WASP, който има предимствата на това, че е негемолитичен и нецитотоксичен. Polybia-MP1 приема a-helical структура, която може да образува стабилен монослой in vivo, да се придържа плътно към повърхността на мембраната, да промени осмотичното налягане и да има бактерициден ефект. За Polybia-MP1 балансът между общите атрактивни и отблъскващи взаимодействия може да бъде прецизиран от хидродинамична якост и рН и тъй като този ефект е свързан с лизин и аспарагинова киселина, подобни ефекти могат да възникнат в други пептидни последователности, съдържащи тези остатъци.
Спецификации
Аперанция: бял до бял прах
Чистота (HPLC): ≥98.0%
Единична примес: ≤2.0%
Съдържание на ацетат (HPLC): 5.0%~12.0%
Водно съдържание (Karl Fischer): ≤10.0%
Съдържание на пептиди: ≥80.0%
Опаковане и доставка: Ниска температура, вакуумна опаковка, точна до MG според нуждите.
Как да поръчате?
1. Свържете се с нас директно по телефон или имейл: +86-13735575465, sales1@gotopbio.com.
2. Поръчайте онлайн. Моля, попълнете онлайн формуляра за поръчка.
3. Предоставете име на пептид, CAS № или последователност, чистота и модификация, ако е необходимо, количество и др. Ще предоставим оферта в рамките на 2 часа.
4. Конформация на поръчка от надлежно подписан договор за продажби и NDA (споразумение за несъответствие) или поверително споразумение.
5. Ние непрекъснато ще актуализираме напредъка на поръчката във времето.
6. Пептидът от DHL, FedEx или други, и HPLC, MS, COA ще бъдат осигурени заедно с товара.
7. Политиката за възстановяване на възстановяването ще се спазва, ако някакво разминаване на нашето качество или услуга.
8. Услуга след продажба: Ако нашите клиенти имат въпроси относно нашия пептид по време на експеримента, не се колебайте да се свържете с нас и ние ще отговорим на него за кратко време.
Всички продукти на компанията се използват само за научни изследвания, ИТ’S забранено да се използва директно от всички индивиди върху човешкото тяло.
Често задавани въпроси:
Дали пептидите, съдържащи Cys, бяха ли намалени преди изпращане?
Ако не се установи, че пептидът е окислен, ние обикновено не намаляваме CYS. Всички полипептиди се получават от сурови продукти, пречистени и лиофилизирани при PH2 условия, което поне до известна степен предотвратява окисляването на Cys. Пептидите, съдържащи Cys, се пречистват при PH2, освен ако няма конкретна причина за пречистване при PH6.8. Ако пречистването се извършва при PH6.8, пречистеният продукт трябва да се третира незабавно с киселина, за да се предотврати окисляването. В крайния етап на контрол на качеството, за пептидите, съдържащи Cys, ако присъствието на молекулно тегло (2p+H) се намира на MS MAP, това показва, че е образуван димер. Ако няма проблем с MS и HPLC, ние директно ще се лиофилизираме и изпращаме стоките без никаква допълнителна обработка. Трябва да се отбележи, че пептидите, съдържащи Cys, претърпяват бавно окисляване с течение на времето, а степента на окисляване зависи от пептидната последователност и условията на съхранение.
Как да определите дали пептидът е цикъл?
Използваме реакцията на Ellman, за да проверим дали образуването на пръстен е завършено. Ако тестът на Елман е положителен (жълт), реакцията на пръстена е непълна. Ако резултатите от теста са отрицателни (не са жълти), реакцията на пръстена е завършена. Ние не предоставяме доклада за анализ на идентификацията на циклизацията за нашите клиенти. Като цяло ще има описание на резултатите от тестовете на Елман в доклада за QC.
Имам нужда от цикличен пептид, който съдържа триптофан, ще бъде ли окислен?
Окисляването на триптофана е често срещано явление при пептидно окисляване и пептидите обикновено се циклират преди пречистване. Ако се случи окисляването на триптофана, времето на задържане на пептида върху колоната HPLC ще се промени и окисляването може да бъде отстранено чрез пречистване. Освен това, окислените пептиди могат да бъдат открити и от МС.
Необходимо ли е да се постави пропаст между пептида и багрилото?
Ако ще прикрепите голяма молекула (като багрило) към пептида, най -добре е да поставите пространство между пептида и лиганда, за да се сведе до минимум смущения с рецептора чрез сгъването на самия пептид или чрез сгъването на неговия конюгат. Други не искат интервали. Например, при сгъването на протеините е възможно да се определи колко далеч се отделя структурата на сгъваемата аминокиселина чрез прикрепване на флуоресцентно багрило към определено място.
Ако искате да направите биотин модификация на N терминала, трябва ли да поставите празнина между биотин и пептидната последователност?
Стандартната процедура за етикетиране на биотин, използвана от нашата компания, е да прикачи AHX към пептидната верига, последвана от биотин. AHX е 6-въглеродно съединение, което действа като бариера между пептида и биотин.
Можете ли да дадете някои съвети относно дизайна на фосфорилирани пептиди?
С увеличаването на дължината ефективността на свързване постепенно намалява от фосфорилираната аминокиселина нататък. Посоката на синтеза е от терминал C до N терминала. Препоръчва се остатъците след фосфорилираната аминокиселина да не надвишават 10, тоест броят на аминокиселинните остатъци преди фосфорилираната аминокиселина от терминала N до терминала на С не трябва да надвишава 10.
Защо N-крайното ацетилиране и С-крайната амидиране?
Тези модификации предотвратяват разграждането на пептида и позволяват на пептида да имитира първоначалното си състояние на алфа амино и карбоксилни групи в родителския протеин.

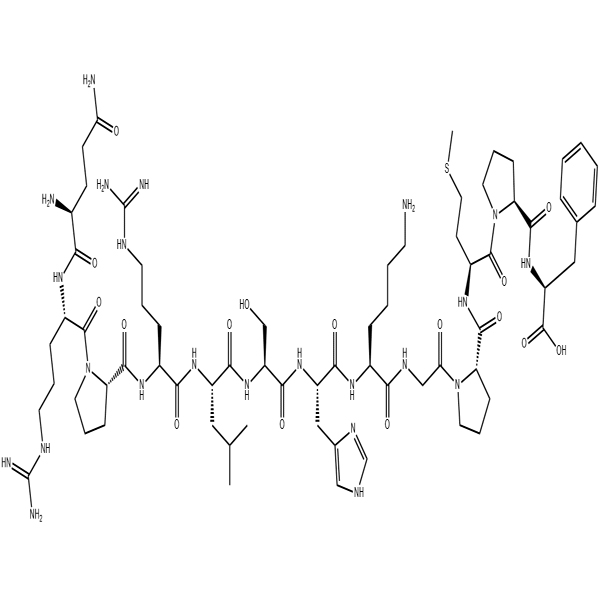
![[SER140]-PLP(139-151)/122018-58-0 /GT Peptide/Peptide Supplier](https://www.gtpeptide.com/uploadfile/202506/42e12ad000f1f04.jpg)