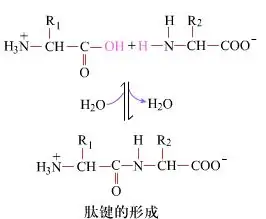
На повърхността образуването на пептидни връзки, получаващи дипептиди, е прост химичен процес. Това означава, че двата компонента на аминокиселини са свързани с пептидна връзка, амидна връзка, докато се дехидратират.
Образуването на пептидна връзка е активирането на аминокиселина при леки реакционни условия. (А) Карбоксилна част, втора аминокиселина (В) нуклеофилната активирана карбоксилна част след това образува дипептида (A-B). „Ако карбоксилният компонент (А) не е защитен, образуването на пептидната връзка не може да бъде контролирана.“ Странични продукти като линейни и циклични пептиди могат да се смесват с целеви съединения A-B. Следователно, всички функционални групи, които не участват в образуването на пептидна връзка, трябва да бъдат защитени по временно обратим начин по време на синтеза на пептиди.
И така, пептидният синтез - образуването на всяка пептидна връзка - включва три етапа на агрегация.
Първата стъпка е да се приготвят някои аминокиселини, които се нуждаят от защита, а zwitterionic структурата на аминокиселините вече не съществува.
Вторият етап е двуетапна реакция за образуване на пептидни връзки, при която карбоксилната група на N-защитената аминокиселина първо се активира към активния междинно съединение и след това се образува пептидната връзка. Тази свързана реакция може да възникне или като реакция от една стъпка, или като две последователни реакции.
Третата стъпка е селективното отстраняване или пълно отстраняване на защитната основа. Въпреки че цялото отстраняване може да се случи само след сглобяване на всички пептидни вериги, се изисква и селективно отстраняване на защитни групи, за да се продължи синтезът на пептидите.
Тъй като 10 аминокиселини (Ser, Thr, Tyr, Asp, Glu, Lys, Arg, His, Sec и Cys) съдържат функционални групи на страничната верига, които изискват селективна защита, което прави синтеза на пептид по -сложен. Временните и полу постоянни бази за защита трябва да се разграничат поради различните изисквания за селективност. Временните групи за защита се използват в следващата стъпка за отразяване на временната защита на аминокиселини или карбоксилни функционални групи. Полу-постоянните защитни групи се отстраняват, без да се намесват във вече образувани пептидни връзки или странични вериги на аминокиселини, понякога по време на синтеза.
„В идеалния случай активирането на карбоксилния компонент и последващото образуване на пептидни връзки (реакции на свързване) трябва да бъде бързо, без рацемично или образуване на странични продукти, а моларните реагенти трябва да се прилагат за постигане на високи добиви.“ За съжаление, нито един от методите за химическо свързване не удовлетворява тези изисквания, а малцина не са подходящи за практически синтез.
По време на синтеза на пептиди функционалните групи, участващи в различни реакции, обикновено са свързани с ръчния център, като глицинът е единственото изключение и съществува потенциален риск от въртене.
Последната стъпка в цикъла на синтеза на пептиди е отстраняването на всички защитни групи. Селективното отстраняване на защитни групи е важно за удължаване на пептидната верига в допълнение към изискването за пълно отстраняване на защитата в дипептидния синтез. Синтетичните стратегии трябва да бъдат внимателно планирани. В зависимост от стратегическия избор, N може избирателно да премахне групите за защита на α-амино или карбоксил. Терминът „стратегия“ се отнася до последователността на кондензационните реакции на отделните аминокиселини. Като цяло има разлика между постепенната синтеза и кондензацията на фрагменти. Пептидният синтез (известен също като „конвенционален синтез“) се осъществява в разтвор. В повечето случаи постепенното удължаване на пептидната верига може да бъде синтезирано само чрез използване на пептидната верига за синтезиране на по -къси фрагменти. За да се синтезират по -дълги пептиди, целевите молекули трябва да бъдат сегментирани в подходящи фрагменти и да определят, че те могат да сведат до минимум степента на диференциация на С края на С. След като отделните фрагменти постепенно се сглобяват, целевото съединение ще бъде съединено. Стратегията на синтеза на пептид включва избора на най -добрия и най -подходящ защитен фрагмент, а стратегията на синтеза на пептид включва избора на най -подходящата комбинация от защитни основи и най -добрият метод за конюгиране на фрагменти.
Време за публикация: 2025-07-02